..:::: درمان زخمها با استفاده از شکر ::::..
پژوهش جدید دانشمندان دانشگاه وولورهامپتون نشان داد که طب سنتی آفریقایی ممکن است از کلید درمان زخمهایی برخوردار باشد که با طب مدرن در تضاد است. طبق این درمان، ریختن شکر ریز بر روی زخمهای بد مانند زخم پا یا حتی قطع عضو میتواند فرآیند درمان را در زمان شکست آنتیبیوتیکها و درمانهای دیگر ارتقا بخشد. این پژوهش توسط موسی موراندو، مدرس ارشد دانشکده پرستاری بزرگسالان در دانشگاه وولورهامپتون انجام شده که در زیمباوه رشد کرده و پدرش در زمان بچگی از شکر برای ترمیم زخمها و کاهش درد استفاده میکرده است. شکر آب را از زخم به یک پارچه انتقال داده که محیط مورد نیاز باکتری برای رشد را از بین میبرد و فرآیند بهبود زخم را تسریع میکند. تاکنون 35 بیمار که از این درمان بهرهمند شدهاند، با بهبود شرایط خود مواجه شده و هیچگونه عوارض جانبی نیز گزارش نشده است. این درمان از این رو موفق بوده که باکتری برای رشد به آب نیاز دارد از این رو قرار دادن شکر بر روی زخم باعث کشیدن آب شده و محیط مناسب رشد باکتری را از بین میبرد.
..:::: ترمیم درد مفاصل با تزریق خون ارتقا یافته ::::..
دانشمندان درحال بررسی درمان درد مفاصل با تزریق خون به زانوی بیمار هستند. در این درمان سعی بر این است که سطوح یک ترکیب طبیعی موسوم به گیرنده آنتاگونیست اینترلوکین1 افزایش یابد. تصور میشود که این ترکیب نقش مهمی در کاهش التهاب داشته باشد. دانشمندان بر این باورند که مقدار کاهش یافته این آنتاگونیست با فروپاشی غضروف در مفاصل مرتبط است. در این درمان جدید، خون از دست بیمار گرفته شده و در یک انکوباتور که با دانههای شیشهای ویژه طراحی شده است، قرار داده میشود. این دانهها به تولید واکنشی که سطوح ترکیب اینترلوکین1 را در یک دوره 9 ساعته افزایش داده، کمک میکند. این خون سپس از دستگاه خارج شده و دوباره طی شش تزریق به بیمار برگردانده میشود. پژوهشهای ابتدایی بر روی گروه کوچکی از بیماران نشان داد که این تزریقها میتوانند پس از یک دوره سه ماهه درد را تسکین داده و حرکت فرد را ارتقا بخشند.
..:::: چربی قهوهای، امید تازه درمان چاقی ::::..
پژوهشگران دانشگاه اوتاوا مکانیزمی را کشف کردهاند که طی آن سلولهای بنیادی عضله به چربی قهوهای تبدیل میشود؛ این نوع چربی نقش جدی را در مبارزه با چاقی ایفا میکند. براساس گزارش سازمان سلامت جهانی، چاقی به عنوان پنجمین عامل مرگ در سراسر جهان به شمار میرود که به طور آماری سالانه حدود 2.8 میلیون نفر در جهان به علت تاثیرات اضافه وزن بر وضعیت سلامتیشان، جان خود را از دست میدهند. دکتر "مایکل رودنیکی"، سرپرست این پژوهش و رییس مرکز تحقیقات ژنتیک مولکولی کانادا طی این مطالعه برای نخستین بار نشان داده است که سلولهای بنیادی عضله نه تنها توانایی تولید فیبرهای عضلانی را دارند بلکه قابلیت تبدیل به چربی قهوهای را نیز دارند.
چربی قهوهای، بافت چربی سوزی است که در گرم نگه داشتن و تنظیم دمای بدن نقش مهمی را ایفا میکند. علاوه بر این وجود هرچه بیشتر چربی قهوهای با کاهش هرچه بیشتر چاقی مرتبط است. نکته اصلی در روند تبدیل سلول بنیادی عضله به چربی قهوهای، تنظیم کننده ژنی به نام "microRNA-133" است که به هنگام حضورش، سلولهای بنیادی به فیبرهای عضلانی تبدیل میشوند و زمانی که کاهش مییابد، سلولهای عضلانی به چربی قهوهای تبدیل میشوند.
دانشمندان طی این پژوهش نشان دادند زمانی که به موشهای بالغ عامل کاهش دهنده "microRNA-133" موسوم به "الیگو نوکلئوتید آنتی سنس ASO" تزریق میشود، چربی قهوهای بیشتری را تولید میکنند که موجب حفاظت بدن از چاقی و بهبود توانایی بدن در پردازش قند خون میشود. علاوه بر این، پس از چهار ماه نیز مشاهده شد که تزریق "ASO" به عضله پای عقبی موش باعث افزایش تولید انرژی کل بدن میشود. محققان خاطرنشان کردهاند که گرچه نتایج به دست آمده جالب و چشمگیر است، اما هنوز در مراحل ابتدایی به سر میبرد و تحقیقات زیادی برای تایید قطعی و سووالات زیادی که در پی این نتایج مطرح میشود، لازم است. این تحقیق در مجله معتبر "Cell Metabolism" منتشر شده است.
..:::: تولید نانوذراتی جدید و ارزان برای درمان سرطان ::::..
پژوهشگران موسسه فناوری سلطنتی ملبورن، نانوذراتی تولید کردهاند که بسیار ارزان و غیرسمی بوده و از آن میتوان برای رادیودرمانی سرطان استفاده کرد. این نانوذرات میتواند جایگزین نانوذرات گرانقیمت طلا در درمان سرطان شود. این تیم تحقیقاتی استرالیایی روی یافتن جایگزینی برای نانوذرات طلا کار میکنند تا از آن در درمان سرطان استفاده کنند. نانوذرات طلا بسیار گرانقیمت و تا حدی سمی است. محمود القطامی میگوید: ما دریافتیم که بیسموت میتواند گزینه ایدهآلی باشد. تستهای ما نشان داد اگر از نانوذرات بیسموت استفاده شود، مقدار تابش دو برابر شده و سلولهای سرطانی از بین میروند. در واقع اگر مقدار تابش را بتوان افزایش داد، آن گاه میتوان مقدار دوز ماده رادیودرمانی را کاهش داد؛ با این کار بیمار کمتر در معرض اثرات منفی این داروها قرار میگیرد. وی میافزاید: نانوذرات فلزی میتوانند موجب بهبود و افزایش کارایی رادیودرمانی شوند، اما باید از موادی ارزانتر و ایمنتر برای این کار استفاده کرد.
نانوذرات بیسموت گزینه مناسبی برای این کار است، زیرا قیمت هر گرم آن تنها چند دلار است، در حالی که هر گرم نانوذرات طلا هزاران دلار قیمت دارد. از سوی دیگر نانوذرات بیسموت غیرسمی بوده و عوارض جانبی اندکی دارد. القطامی میگوید: با این حال هنوز باید تحقیقات بیشتری در این باره انجام داد تا بتوان از این سیستم در درمان سرطان استفاده کرد. نتایج این پژوهش بسیار جالب توجه بوده و انگیزههای ما را برای ادامه تحقیقات افزایش میدهد.
القطامی با چند گروه تحقیقاتی از دانشگاه ملبورن، موسسه تحقیقاتی سلامت در موسسه فناوری سلطنتی ملبورن، دانشگاه سری و موسسه تحقیقات سرطان برای انجام این پروژه همکاری داشته است. برای تست کارایی بیسموت، القطامی نانوذرات بیسموت را درون یک شناساگر قرار داد؛ شناساگری که توسط همین گروه تحقیقاتی ساخته شده بود. آنها با استفاده از این شناساگر مقدار دوز تابش را در سه بعد اندازهگیری کردند.
محققان نمونه و شناساگر را در معرض تابش نرمال مورد استفاده در درمان سرطان قرار دادند. مقدار تابش مورد نیاز برای رهاسازی در نانوذرات بیسموت با دوز مورد نیاز برای درمان با نانوذرات طلا مقایسه شد. نتایج نشان داد که نانوذرات مبتنی بر بیسموت تابش را 90 درصد افزایش میدهند. این تیم تحقیقاتی قصد دارد که مطالعات بیشتری انجام دهد تا یافتههای خود را اعتبار بیشتری ببخشد. با این کار مسیر استفاده از این روش برای درمان سرطان هموار میشود. نتایج این پژوهش در کنفرانس بین المللی دوزیمتری تابش سه بعدی در سیدنی ارائه شده است.
..:::: درمان سرطان با نانوحبابهای پلاسمونیک ::::..
محققان دانشگاه رایس روشی ارائه کردهاند که با استفاده از آن میتوان برخی سلولهای بیمار را از بین برد و برخی دیگر را درمان کرد. این فرآیند با استفاده از پرتو لیزر پالسی فعال شده و میتوان با استفاده از آن برخی سلولها را تحت تاثیر قرار داد، در حالی که سلولهای مجاور سلول مورد نظر بدون تغییر باقی بمانند. در این روش از نانوحبابهای پلاسمونیک قابل تنظیم استفاده شده است که میتواند جایگزینی مناسبی برای روشهای چند مرحلهای فعلی برای درمان سرطان باشد. همچنین این روش جدید بسیار سریعتر است.
نانوحبابهای پلاسمونیک دههزار برابر کوچکتر از قطر تار موی انسان هستند که میتوانند بترکند. زمانی که نانوذرات طلا در معرض تابش لیزر با قدرت بالا قرار گیرند، حبابهایی در اطراف آنها ایجاد میشود. این حبابها که در اثر تبخیر یک لایه محلول اطراف نانوذرات ایجاد میشوند، عمر کوتاهی داشته و به سرعت میترکند. «لاپوتکو» و همکارانش دریافتند که این نانوحبابهای پلاسمونیک قادرند سلولهای سرطانی را از بین ببرند، بدون این که به سلولهای سالم آسیبی وارد شود. «لاپوتکو» میگوید: این روش بسیار دقیق است و از نظر دقت و انتخابگری بسیار بهتر از زمانی است که تنها از نانوذرات طلا استفاده میشود.
این پژوهش قدمهای رو به جلوی قابل توجهی برای درمان سرطان برداشته است. یکسِری آزمایشات درباره عملکرد این روش انجام شده است که در آن از لیزرهای پالسی برای ایجاد نانوحباب پلاسمونیک استفاده شده است، نانوحبابهایی که در اطراف نانوذرات توخالی تشکیل میشود. نتایج این آزمایشها نشان میدهد که این نانوحبابها قادرند سلولهای ناخواسته را به صورت انتخابی از بین ببرند. همچنین این لیزر میتواند در اطراف نانوکرههای طلا نانوحبابهایی ایجاد کند، این نانوحبابها موجب فشار روی دیواره سلول شده و با استفاده از آن دارو یا ژن به درون سلول تزریق میشود.
در یک آزمایش، محققان از نانوذرات توخالی 60 نانومتری استفاده کرده و سلولهای سرطانی را به رنگ قرمز در آوردند، در آزمایش دیگری آنها همان نوع سلولها را به رنگ آبی در آوردند. سپس این سلولها را با هم ترکیب کرده و در معرض تابش لیزر قرار داده تا رنگ سبز از بین برود. مشاهدات میکروسکوپی نشان داد که سلولهای قرمز در اثر نانوحبابهای پلاسمونیک بزرگ از بین رفتهاند، اما سلولهای آبی که در معرض نانوحبابهای کوچک بودند، دستنخورده باقی مانده و مقداری مایع سبز درون آنها وارد شده بود.
تشخیص و درمان آرتريت روماتوييد
آرتريت روماتوييد شايعترين بيماري التهابي سيستميک مفاصل است که تاکنون شناخته شده است. زنان، سيگاريها و افراد داراي سابقه خانوادگي مثبت بيشتر به اين بيماري مبتلا ميشوند. معيارهاي تشخيصي شامل درگيري حداقل يک مفصل همراه با تورم مشخصه آن است که با بيماري ديگري قابل توجيه نباشد. احتمال تشخيص آرتريت روماتوييد با افزايش تعداد مفاصل کوچک درگير افزايش مييابد. در افراد مبتلا به آرتريت التهابي وجود عامل روماتوييد (RF) يا آنتيبادي ضد پروتئين سيترولينه (ACPA) يا افزايش پروتئين واکنشي CRP) C) يا سرعت رسوب گلبولهاي قرمز (ESR) به نفع تشخيص آرتريت روماتوييد است. ارزيابي اوليه آزمايشگاهي بايد شامل شمارش کامل سلولهاي خون (CBC) همراه با شمارش افتراقي (diff) و بررسي کارکرد کبد و کليه باشد. بيماراني که داروهاي بيولوژيک دريافت ميکنند بايد از نظر هپاتيت B و C و سل بررسي شوند. تشخيص آرتريت روماتوييد در مراحل اوليه، شروع زودهنگام درمانهاي ضد روماتيسمي تعديلکننده سير بيماري(1) (DMARDها) را امکانپذير ميکند.
..:::: درمان سرطان با نوعی قارچ انگل ::::..
قارچ «oligospora» میتواند نوعی نانوذره تولید کند که باعث تحریک سیستم ایمنی بدن شده و در نهایت سیستم ایمنی بدن، سلولهای سرطانی را از بین میبرند. «oligospora» نام نوعی قارچ است که زندگی جذابی ندارد، بلکه به عنوان یک انگل در بدن میزبان زندگی میکند. اما اخیرا تیم تحقیقاتی به رهبری «مینگیم ژانگ»، استادیار رشته زیست پزشکی دانشگاه تنسا دریافتهاند که این قارچ میتواند برای درمان سرطان مفید باشد.
«ژانگ» همیشه به نحوی به طبیعت نگاه میکند که از آن برای حل مشکلات جهانی استفاده کند. او و دستیارش «یونگژانگ»، «Arthrobotrys oligospora» را مورد مطالعه قرار دادند؛ نتایج مشاهدات آنها نشان داد که نانوذرات با ابعاد یکنواخت توسط این قارچ تولید میشود. نتایج تحقیقات بعدی حکایت از این حقیقت داشت که نانوذرات تولید شده توسط قارچ میتواند برای درمان سرطان مورد استفاده قرار گیرد. «ژانگ» میگوید: نانوذراتی که به صورت طبیعی ایجاد میشوند، به دلیل زیست سازگار بودن بسیار مورد توجه دانشمندان است. به دلیل نسبت سطح به حجم بالا، نانوذرات دارای خواص نوری، گرمایی و الکتریکی ویژهای هستند. علاوه براین به دلیل ابعاد بسیار کوچک این ترکیبات، ورود و خروج آنها از غشاء سلولی بسیار ساده انجام میشود. این ویژگیها برای تولید داروی ضد سرطان ضروری است.
این تیم تحقیقاتی به بررسی پتانسیل نانوذرات تولید شده توسط این قارچ پرداختند؛ این نانوذرات قادر است سیستم ایمنی بدن را تحریک کند. نتایج تحقیقات آنها نشان داد که این نانوذرات میتوانند موجب ترشح یک ماده از گلبولهای سفید خون شوند. «ژانگ» میگوید: طبیعت در مواجهه با بیماریهای مختلف مکانیسمهای فوقالعادهای را برای درمان آنها پیشنهاد می کند. تعداد بیشماری نانوساختار طبیعی وجود دارد که هر یک میتواند ابزاری جدید برای درمان بیماریها باشد. نتایج این پژوهش میتواند درگاهی برای وارد شدن به یک معدن طلا باشد؛ معدنی که مملو از مواد جدید برای درمان سرطانها است. فهم این که این نانوساختارها در سیستم طبیعی چگونه تولید میشوند، الگویی است برای سنتز نسل جدید نانومواد مهندسی شده جهت درمان بیماریها. راهبرد مورد استفاده در این پروژه مسیر تازهای به سوی کنترل سنتز نانوذرات آلی باز میکند. این کشف جالب توجه اولین قدم به سوی توسعه داروهای مبتنی بر نانوذرات طبیعی است؛ داروهایی که برای درمان سرطان مناسب هستند. این پژوهش توسط برنامه زیست شیمی ارتش آمریکا حمایت مالی شده است. نتایج این پژوهش در نشریه «Advanced Functional Materials» به چاپ رسیده است.
..:::: درمان آرتروز زانو بوسیله پلاسمای غنی از پلاکت ::::..
در مقاله که درمجله بالینی Sports Medicine به چاپ رسیده است، محققان بخش جراحی بیمارستان نشان دادند که پلاسمای غنی از پلاکت (PRP) می تواند به درمان بیماران مبتلا به آرتروز زانو کمک کند.این درمان می تواند باعث بهبود درد و عملکرد زانو وهمچنین در %75 درصد بیماران مانع پیشرفت بیماری شود. درمان های مختلفی برای آرتروز وجود دارد که از جمله این درمان ها می توان به ورزش کردن، کنترل وزن، استفاده از داروهای غیر استروئیدی ضد التهابی ، تیلنول، کورتیزول و روش تزریق ماده ژل مانند به زانو به عنون روان کننده طبیعی در مفصل اشاره کرد. درمان جدیدی که اخیرا توسط تعداد کمی از پزشکان مورد مطالعه قرار گرفته است، روش درمانی تزریق (PRP) می باشد.پلاسمای غنی شده از پلاکت (PRP) که از خون خود بیمار گرفته می شود دارای غلظت بالایی از فاکتورهای رشد است که می تواند باعث بهبود التهاب مفاصل شود.
به گفته دکتر Halpern در این روش ابتدا از فرد مقداری نمونه خون گرفته می شود و سپس طی مراحلی پلاکت ها جدا شده و با غلظت بالا به زانوی خود فرد تزریق می شود.این پلاکت های تزریق شده باعث فعال شدن سلول های بنیادی و عوامل رشد شده که به نوبه خود می تواند باعث کاهش علائم آرتروز و التهاب مفاصل شود. محققان در مطالعه انجام شده ، بیماران مبتلا به آرتروز اولیه را مورد بررسی قرار دادند.در این آزمایش به این بیماران 6ML از پلاسمای غنی از پلاکت (PRP) تزریق شد و سپس بیماران به مدت یکسال از نظر درد ، خشکی و عمکرد زانو و توانایی انجام فعالیت های مختلف روزمره مورد ارزیابی قرار گرفتند. یک سال پس از تزریق ارزیابی توسط تصویر برداری (MRI) نیز انجام شد و نتایج رضایت بخش بود.
در حالی که مطالعات قبلی نشان داده اند که بیماران مبتلا به آرتروز در هر سال حدود %5 درصد از غضروف زانوی خود را از دست می دهند ،در مورد اکثریت بیماران در این مطالعه هیچ گونه کاهش یا ازدست غضروفی گزارش نشده است. درمان به روش PRP هم در بهبود درد و سفتی و هم دربهبود عمکرد بسیار مفید می باشد.محققان دراین مطالعه توسط دو آزمون استانداردWestern Ontario و Arthritis Index McMaster Universities میزان درد را در بیماران مورد سنجش قرار دادند. نتایج نشان داد که میزان درد در شش ماه اول %41.7 و در شش ماه دوم %55.9 درصد کاهش داشته است.همچنین میزان فعالیت زندگی روزانه نیز به طور قابل توجهی در هر دو شش ماه (%46.8) و یک سال (%55.7) افزایش نشان داد.
دکتر Halpern درمورد این نوع درمان گفت : ما در حال ورود به دوره فوق العاده ای از درمان های بیولوژیک هستیم که در آن به جای استفاده از مواد مصنوعی از سلول های خودمان برای ترمیم سلول های خود بهره می بریم.دکتر Halpern در انتها به این موضوع اشاره کرد که: روش PRP در حد آزمایشگاهی انجام شده است و باید با درمان های سنتی مورد مقایسه قرار بگیرد. Osteoarthritis یا آرتروز که باعث درد و سفتی مفاصل می شود ، عامل اصلی ناتوانی و معلولیت بیش از 27 میلیون آمریکایی می باشد.باتوجه به آمار مرکز کنترل وپیشگیری از بیماری ها ، بیماری آرتروز %13.9 درصد از بالغین 25 سال به بالا و %33.6 درصد از افراد مسن بالای 65 سال را مبتلا می سازد.این بیماری از طریق تخریب غضروف و استخوان زیرین آن و همچنین رشد بیش از حد استخوانی مشخص می شود. شروع این بیماری به صورت تدریجی است ومعمولا پس از 40 سالگی آغاز می شود.
..:::: بهبود بینایی افراد دیابتی با تکنولوژی سلول های بنیادی ::::..
دانشمندان دانشگاه Belfast Queen's به دنبال یک رویکرد جدید، به منظور کمک به درمان بینایی میلیون ها نفر از مبتلایان به دیابت ، با استفاده از سلولهای بنیادی بالغ هستند. در حال حاضر میلیون ها نفر از افراد دیابتی درسراسر جهان، در معرض خطر ازدست دادن بینایی خود به علت یک بیماری به نام رتینوپاتی دیابتی می باشند.این بیماری زمانی رخ می دهد که رگ های خونی در چشم ها به علت قند خون بالا مسدود می شوند.قطع جریان خون در شبکیه چشم باعث آسیب رسیدن به سلول های بینایی و اختلال دید می شود و سرانجام در صورت عدم درمان به موقع می تواند منجر به کوری شود.
مطالعه روش جدید ترمیم آسیب های دیابتی توسط سلول های استروما،) که به اختصار (REDDSTAR) نام دارد، برگرفته از تحقیقات دانشمندان مرکز چشم و علوم عروق در دانشکده پزشکی Queen's می باشد. در این روش محققان سلول های بنیادی را از اهدا کنندگان جدا کرده و بعد از گسترش آنها در محیط کشت این سلول ها را به رگ های خونی آسیب دیده بیمار که نیاز به ترمیم دارند تزریق می کنند.این روش مخصوص بیماران مبتلا به دیابتی است که عروق شبکیه در آنها دچار آسیب شده است.
در حال حاضرروش های درمانی اندکی برای کنترل پیشرفت عوارض بیماری دیابت در دسترس است وهمچنین هیچ درمانی برای بهبود همزمان میزان قند خون و عوارض دیابت وجود ندارد. پرفسور Alan Stitt مدیر مرکز چشم و علوم عروقی Queen's در مورد این پروژه گفت : جزئیات مطالعه بر روی روش (REDDSTAR)، شامل بررسی پتانسیل منحصر به فرد سلول های بنیادی برای ترویج ترمیم عروق خونی آسیب دیده در شبکیه چشم دربیماری دیابت می باشد.این موضوع می تواند تاثیر عمیقی بر روی بیماران داشته باشد، زیرا احیاء شبکیه آسیب دیده می تواند از رتینوپاتی دیابتی جلوگیری کند و ریسک از دست دادن بینایی را در این بیماران کاهش دهد.در حال حاضر، درمان های موجود برای رتینوپاتی دیابتی ،همیشه رضایت بخش نبوده است.این درمان ها بر روی مراحل پایانی بیماری تمرکز دارند و دارای عوارض جانبی زیادی هستند و قادر به درمان علل ریشه ای این بیماری نیستند.یک روش جدید جایگزین برای مهار این بیماری بازسازی عروق آسیب دیده شبکیه توسط سلول های بنیادی بالغ می باشد. این پژوهش که بر روی سلول های بنیادی بالغ خاصی که از مغز استخوان مشتق شده متمرکز شده است با حمایت شرکت Orbsen Therapeutics و بنیاد علوم ایرلند ارائه شده است.
..:::: استفاده از سلول های بنیادی دردرمان بیماری های کبدی ::::..
دانشمندان امریکایی ایمنی و کارایی سلول های شبه کبدی یا Hepatocyte-like cell مشتق شده از نوعی سلول بنیادی به نام hpSC رادرمدل حیوانی دچاریک اختلال کبدی مادر زادی با متابولیسم بیلی روبین نشان داده اند. یافته های این گروه تحقیقاتی که در فاز پیش بالینی انجام شده بیان می کند که پیوند HLC در جوندگان بیلی روبین خون را به سرعت کاهش می دهد و در سطح ثابتی نگه می دارد.
سندرم Criggler-Najjar نوع یک یا CN1 یک اختلال متابولیکی ارثی نادر است که در آن کبد مبتلایان فاقد آنزیمی خاصی به نام UGT1A1 است . این آنزیم برای پاک سازی بیلی روبین سمی لازم است. سندرم سبب ایجاد بیش از حد بیلی روبین متصل نشده یا hyperbilirubinemia Unconjugated می شود. این اختلال منجربه مشکلات شدید عصبی می شود که اگر درمان نشوند می توانند باعث آنسفالوپاتی حاد برگشت ناپذیر شوند. با آن که پیوند سلول های کبدی (hepatocyte) یا HI به عنوان گزینه درمانی جایگزین برای افرادی با بیماری های متابولیکی ناشی از کبد نظیر CN1 استفاده می شود اما دارای محدودیت هایی نیز می باشد.
استفاده از HLC برای درمان CN1 دارای مزایایی نسبت به پیوند سلول های کبدی اولیه است. این سلول ها جبران کمبود سلول های اولیه را می کنند همچنین شواهدی وجود دارد که پیوند HLC در مقایسه با سلول های کبدی نابالغ جنینی فعالیت متابولیکی بهتری نشان می دهند.ازHLC ها می توان قبل از شروع آنسفالوپاتی بیلی روبین استفاده کرد در نتیجه با تولید کافی آنزیم UGT1A1 کبد توانایی متابلیزه کدن بیلی روبین را می یابد.علاوه بر این نتایج با گذشت 16 هفته از پیوند،عوارض ناخواسته مشاهده نشده ودر مقایسه با گروه شاهداز میزان بیلی روبین سرم نیز کاسته شده است. ساختار و مورفولوژی کبددر همه جوندگان در مان شده مورد مطالعه سالم و بدون التهاب، تومورزایی و پس زدن پیوند گزارش شده است. دکتر Ruslan Semechkin یکی از اعضای گروه می گوید این مطالعه شواهد مهمی را برای استفاده از محصول HLC به عنوان منبع قابل اعتماد برای سلول های قابل پیوند شدن در درمان CN1 ،فراهم کرده است. با تکمیل این مطالعات ،دانشمندان می توانند تائیدیه های لازم برای کاربرد این سلول ها در فاز اول بالینی را دریافت کنند.
..:::: وياگرا ممکن است به مبارزه با چاقي کمک کند ::::..
پژوهشگران آلماني در دانشگاه بن با دادن داروي وياگرا به موشها کشف کردند اين دارو باعث تبديل سلولهاي چربي سفيد (يعني همان چربي ناخواستهاي که در شکم و جاهاي ديگر بدن جمع ميشود) به سلولهاي چربي قهوهاي ميشود. سلولهاي تازه کشفشده چربي قهوهاي به جاي ذخيره انرژي اضافي، انرژي دريافتشده از غذا را ميسوزانند و آن را به گرما تبديل ميکنند.
به نظر ميرسد وياگرا (حداقل در موشها) خطر عوارض ديگر ناشي از چاقي را نيز کاهش ميدهد. وياگرا (که سيلدنافيل هم ناميده ميشود)، براي درمان اختلال کارکرد نعوظي، پرفشاري خون شريان ريوي به کار ميرود. اين دارو باعث شل شدن عضلات صاف ميشود و به اين ترتيب جريان خون لازم براي ايجاد نعوظ را فراهم ميکند. اثر وياگرا روي بافت چربي در سال 2007 مورد توجه قرارگرفت. تحقيقي در آن زمان نشان داد موشهايي که براي 12هفته وياگرا دريافت کرده بودند، هنگامي که با رژيم غذايي پرچربي تغذيه ميشدند، چاق نميشدند. آنها پس از 7 روز دادن وياگرا به موشها، با حداکثر دوز مجاز براي استفاده انساني، کشف کردند شمار زيادي از سلولهاي چربي سفيد در اين موشها به سلولهاي چربي سالمتر قهوهاي تبديل شدهاند. هنگامي که سلولهاي چربي سفيد انرژي بيشتري ذخيره کنند به جاي تقسيم به سلولهاي بيشتر، چربي بيشتري در سلولهاي موجود ذخيره ميشود. اين روند حداقل تا هنگامي که اندازه آنها به 4 برابر اندازه طبيعي برسد، ادامه پيدا ميکند و پس از اين مرحله نهايتا تقسيم ميشوند.
پيش از اينکه سلولهاي چربي به مرحله تقسيم برسند، بزرگشدن سلولهاي چربي باعث آزاد شدن موادي به نام سايتوکاينها ميشود که بر دستگاه ايمني اثر ميگذارند. در اين مورد سايتوکاينهاي آزادشده از سلولهاي چربي باعث تشديد واکنش ايمني و ايجاد التهاب مزمن ميشوند که در دچار شدن به بيماريهاي مزمن مانند بيماريهاي قلبي- عروقي، ديابت، آرتريت و حتي سرطان نقش دارد. سايتوکاينهاي چربي سفيد، بهخصوص به بافتهاي قلبي آسيب ميزنند. نتيجه کلي اين است که وياگرا ميتواند چربي سفيد را به چربي قهوهاي سوزاننده کالري تبديل کند، مانع از بزرگ شدن سلولهاي چربي شود و ميزان توليد سايتوکاينهاي التهابزا را کاهش دهد. البته معلوم نيست که اين نتايج که در آزمايش روي موشها به دست آمده است، لزوما در مورد انسانها هم صادق باشد. از طرف ديگر، در اين آزمايش از دوزهاي بسيار بالاي وياگرا استفاده شده بود تا بر دستگاه ايمني تاثير بگذارد که معلوم نيست بتوان از اين مقادير در انسانها استفاده کرد.
..:::: کشف سلول های بنیادی و درمان چاقی ::::..
دانشمندان موسسه تحقیقاتی بیمارستان اتاوا موفق به کشف روش تبدیل سلول های بنیادی عضله به چربی قهوه ای شدند. چربی قهوه ای شکلی خوب از چربی است که نقش مهمی در مبارزه با چاقی دارد. با توجه به آمار سازمان جهانی بهداشت ، چاقی هرساله با قربانی کردن 2.5 میلیون نفر، به عنوان پنچمین عامل مرگ ومیر در جهان شناخته می شود.آژانس بهداشت عمومی کانادا ، تخمین می زند که %25 درصد از بزرگسالان در کانادا مبتلا به چاقی هستند.
در مقاله ای که امروز منتشر شد دکتر Rudnicki به همراه تیم تحقیقاتی خود برای اولین بار نشان دادند که سلول های بنیادی عضلات اسکلتی بالغ نه تنها توانایی تولید فیبرهای عضلانی را دارند، همچنین قادر به تبدیل شدن به چربی قهوه ای نیز هستند. سوختن بافت چربی قهوه ای باعث تولید حرارت در بدن می شود و این چربی نقش مهمی درتنظیم درجه حرارت بدن داردو بیشتر بودن این چربی با چاقی کمتر در ارتباط است.
این تیم تحقیقاتی در آزمایش های انجام شده موفق به کشف ژن کوچکی به نام microRNA-133 یا miR-133 شدند که حضور آن باعث تبدیل سلول های بنیادی به فیبر عضلانی و عدم حضورش باعث تبدیل این سلول ها به چربی قهوه ای می شود . آزمایش های دکتر Rudnicki نشان داد که تزریق عامل کاهش دهنده miR-133 با نام (ASO) antisense oligonucleotide باعث تولید بیشتر چربی قهوه ای می شود که به نوبه خود می تواند به عنوان یک عامل جلوگیری کننده از چاقی تلقی شود. دکتر Rudnicki در این باره گفت : درمان با استفاده از ASO و کاهش دادن سطح miR-133 روشی است که در حال حاظر در مراحل آزمایشات کلینکی انسانی است. با این حال در سال های آتی می تواند به عنوان یک درمان بالقوه مورد استفاده قرار گیرد.اگر چه دستیابی به این موضوع موفقیت آمیز بوده است اما بسیاری از سوالات مانند اینکه چه مدت باید از این دارو استفاده شود؟ یا آیا این دارو دارای عوارض جانبی هست یا خیر ؟ وجود دارد که باید برای آنها به دنبال پاسخ باشیم. این یافته های بدست آمده در آزمایشگاه دکتر Michael Rudnicki ، مستقر در موسسه تحقیقاتی بیمارستان اتاوا ، در مجله Cell Metabolism منتشر شد.
..:::: درمان روماتیسم مفصلی با پیوند سلول های CD8+ Treg ::::..
دانشمندان توانسته اند راهکار جدیدی برای درمان بیماری های خود ایمنی ارائه دهند که می تواند بطور موفقیت آمیزی مانع پیشرفت روماتیسم مفصلی در یک نوع موش شود. آن ها امید وارند این روش بتواند از این بیماری و سایر بیماری ها ی خود ایمنی در انسان جلو گیری کند. در این مطالعه از یک نوع سلول سیستم ایمنی به نام سلول های T تنظیم کننده یا CD8+ Treg که آبشار واکنش های التهابی و آسیب به بافت ها و مفاصل را متوقف می کنند، استفاده شده است. این سلول ها توانایی ازبین بردن سلول های ایمنی مضری را که باعث روماتیسم می شود دارند. پیوند این سلول ها با تزریق پروتئینی که باعث شروع واکنش خود ایمنی منجر به روماتیسم می شود، همراه بوده است.آن ها توانسته اند با این روش بیماری را کاملا مهار کنند.
سیستم ایمنی انسان شبکه ای از سلول ها ، بافت ها و اندام هاست که در صورت عملکرد طبیعی به باکتری ها ، ویروس ها، انگل ه ودیگر مهاجمین حمله کرده و آن ها را از بین می برد.در اختلالات خود ایمنی بخش هایی از این سیستم به سلول ها و بافت های سالم حمله می کنند. حد اقل 100 بیماری خود ایمنی شناخته شده اند . این نوع بیماری ها بین زنان شایع ترند. روماتیسم مفصلی در اثر حمله سیستم ایمنی به مفاصل ،باعث ایجاد درد و نیز بد شکل شدن انگشتان می شود.
داروهایی که برای این بیماران تجویز می شود به منظور کاهش التهاب به کار می روند.دارو های جدید عوامل بیولوژیکی هستند که از ترشح سایتو کاین ها جلو گیری می کنند . سایتو کاین ها مواد شیمیایی هستند که در این بیماری باعث حملات اشتباهی سلول های ایمنی می شوند.این نوع درمان تولید سایتوکاین هایی نظیر TNF و IL-1 را مهار می کند.علاوه بر حضور سایتو کاین ها حضور سلول های T یاریگر نیز در بروز واکنش های ایمنی الزامی است.برخی از این سلول ها شاخصی به نام Qa-1 در سطح خود دارند و Qa-1 T helper cell نامیده می شوند..سلول های CD8+ Treg مولکولHsp60 را بر روی Qa-1 T helper cell ها شناسایی کرده و در کاهش فعالیت آن ها تاثیر گذارند. هدف از این روش در مانی ازدیاد سلول های CD8+ Treg است که به کمک بیان Hs60 صورت می گیرد. هدف بعدی این گروه تحقیقاتی به کار گیری ذراتی در مقیاس نانو ست که در سطح آ ن ها Qa-1/Hsp60 تعبیه شده است. نتایج این تحقیق در Journal of Clinical Investigation به چاپ رسیده است.
..:::: کمبود ویتامین D خطر ابتلا به دیابت نوع یک را افزایش میدهد ::::..
سطوح پایین ویتامین D میتواند خطر وقوع دیابت نوع یک را افزایش دهد.گروهی از محققان دانشکده بهداشت عمومی دانشگاه هاروارد با بررسی بیش از 40 میلیون نمونه خون قبل از شروع بیماری و سپس بررسی دوباره افراد طی سالها بعد دریافتند: داشتن سطوح کافی ویتامین D در بزرگسالان جوان ممکن است خطر شروع دیابت نوع یک بزرگسالی را تا 50 درصد کاهش دهد. نتایج حاصل از این تحقیق میافزاید: افراد سالم جوان با سطوح سرمی بالاتر ویتامین D نسبت به کسانی که در سطوح سرمی پایینتر ویتامین D بودند، تنها در معرض نیمی از خطر افزایش دیابت نوع یک قرار گرفتند.
محققان با اشاره به یافتههای حاصل از این تحقیق اظهار کردند: مطالعات قبلی نیز نشان دادهاند که کمبود ویتامین D ممکن است بروز دیابت نوع یک را تقویت کند و اگرچه مطالعات بیشتر به بررسی بین میزان ویتامین D در دوران بارداری و یا دوران کودکی و خطر ابتلا به دیابت نوع یک پرداخته است، اما تحقیقات دیگر در بزرگسالان جوان نیز ارتباط بین مقادیر بالای ویتامین D و کاهش خطر ابتلا به ام اس را نیز بررسی کرده است و در واقع مطالعات نشان میدهد که مقادیر ناکافی ویتامین D در دوران بزرگسالی به طور کلی میتواند یک عامل خطر مهم برای بروز بیماریهای خودایمن باشد.
به گفته محققان، یک میلیارد نفر در جهان دارای سطوح ناکافی ویتامین D در خون خود هستند و این کمبود در تمام اقوام و گروههای سنی یافت میشود و در حالی که قرار گرفتن در معرض آفتاب منبع بسیار خوبی از ویتامین D است، اما کرمهای ضد آفتاب، لباسها، رنگ پوست و ماههای زمستانی باعث کاهش تولید ویتامین D میشوند که در این میان برای پیشگیری از دیابت نوع یک استفاده روزانه از مکملهای ویتامین D به افرادی که دچار کمبود آن هستند، توصیه میشود. یافتههای این تحقیق، در نشریه آمریکایی اپیدمیولوژی منتشر شده است.
..:::: پیوند ریه افراد سیگاری به بیماران نیازمند خطری ندارد ::::..
میزان امید به زندگی بیماران پیوند ریه که ازسیگاری های قهار ریه دریافت می کنند، به اندازه بیمارانی است که از افراد غیر سیگاری ریه می گیرند. دانشمندان می گویند، پیوند ریه از اهدا کننده ای که روزی 20 نخ سیگار می کشد، خطری ندارد.نتیجه این مطالعه می تواند به کاهش کمبود اعضای اهدایی کمک کند.
گروهی از محققان بیمارستان دانشگاهی تمپل در فیلادلفیا، اطلاعات حدود 6هزار بیمار را که در فاصله زمانی سال های 2005 و 2010 دو پیوند ریه دریافت کرده بودند تجزیه و تحلیل کردند. از هر هشت عضو اهدایی یک عضو از اهدا کننده ای بود که بیش از 20 سال روزی یک پاکت سیگار می کشید اما در زمان اهدای عضو علائمی از بیماری نداشتند. در این مطالعه محققان متوجه شدند که امید به زندگی بیمارانی که از سیگاری های قهار ریه دریافت کرده بودند به اندازه بیمارانی بود که از افراد غیر سیگاری ریه گرفته بودند. هر دو گروه این بیماران پس از پیوند ریه طول زندگی کوتاه و متوسط داشتند.
به گفته محققان، عملکرد ریه پیوندی زمانی که از سیگاری های قهار اهدا می شود بد نیست و خطر مرگ دریافت کننده را بر اثر ابتلا به سرطان افزایش نمی دهد. دکتر ˈشارون تاگاویˈ از بیمارستان دانشگاهی فیلادلفیا گفت: یافته های ما نشان می دهند که بالقوه می توان در معیارهای فعلی پیوند ریه تجدید نظر کرد و دریافت ریه از اهدا کننده هایی که سابقه سیگار کشیدن زیاد دارند را نیز به آن اضافه کرد. این موضوع می تواند کمبود ریه های اهدایی را برطرف سازد و مرگ و میر ناشی از قرار گرفتن در فهرست انتظار برای پیوند ریه را کاهش داد. پیوند ریه بر روی افرادی انجام می شود که احتمال دارد در عرض دو سال بر اثر بیماری ریوی جان خود را از دست بدهند. این مطالعه در نشست سالانه انجمن جراحان توراکس در لس آنجلس ارائه شد.
..:::: ارتباط بین مصرف قند و خطر وقوع سرطان ::::..
مصرف بیش از حد قند و وقوع دیابت میتواند باعث افزایش بروز سرطان در افراد شود. محققان آکسفورد با انجام تحقیقات خود توانستند یک مکانیسم کلیدی را کشف کنند که نشان میدهد دیابت و چاقی با افزایش خطر ابتلا به سرطان مرتبط است. محققان با مطالعه چگونگی پاسخ سلولهای روده به قندها و سیگنالدهی آنها به ترشح انسولین در لوزالمعده و نیز بررسی انتشار هورمون GIP که باعث افزایش ترشح انسولین میشود، دریافتند: توانایی سلولهای روده به ترشح GIP توسط یک پروتئین به نام b-Catenin صورت میگیرد که افزایش فعالیت این پروتئین به عنوان یک عامل اصلی در توسعه بسیاری از سرطانها شناخته شده است.
نتایج حاصل از این تحقیق نشان میدهد: فعالیت b-Catenin به شدت به سطوح قند وابسته است که در این میان سطوح بالای قند موجب تجمع b-Catenin میشود. به گفته محققان، تغییر در رژیم غذایی یکی از سادهترین استراتژیهای پیشگیری است که به طور بالقوه میتواند باعث کاهش ابتلا به این بیماریها شود. جمعیت دیابتی در مقایسه با بقیه تا دو برابر بیشتر ممکن است از سرطان پانکراس رنج ببرند و یا به سرطان کولون مبتلا شوند.
..:::: درمان آرتروز زانو با تولید ژل از سلولهای بنیادی خون بندناف ::::..
محققان دانشگاه راش در حال استفاده از نوعی ژل ساخته شده از سلولهای بنیادی خون بند ناف برای درمان ورم مفاصل زانو هستند که به گفته آنها، این شیوه به ترمیم و رشد مجدد غضروف آسیبدیده کمک کرده است. یک پژوهش کوچک نشان داد که این درمان به 67 درصد پیشرفت در ترمیم غضروف کمک کرده و محققان بر این باورند که که این روش میتواند جایگزین عمل جراحی تعویض مفصل شود. این درمان از یک داروی پیشگامانه موسوم به «Cartistem» استفاده میکند. Cartistem ترکیبی از سلولهای بنیادی خون بند ناف با پلیمر طبیعی هیالورونان است که نقش مهمی در بهبود زخم ایفا کرده و همچنین یکی از اجزای اصلی غضروف مفاصل است.
این درمان را میتوان برای غضروف آسیبدیده پس از عمل جراحی آرتروسکوپی به عنوان یک مکمل عمل در شیوه ریزترک مورد استفاده قرار داد که یکی از شیوه های معمول برای ترمیم غضروف است. غضروف مانند یک جاذب شوک عمل کرده و یک سطح نرم را ارائه میکند که سر خوردن نرم استخوانها بر روی یکدیگر را ممکن میسازد. با این حال این لایه ممکن است در اثر پیری از بین رفته و باعث درد و ورم و ایجاد بیماری آرتروز میشود.
این بافت مانند دیگر بافتهای بدن در زمان آسیب نمیتواند به سرعت خود را ترمیم کند چرا که از رگهای خونی و عصبی کمی برخوردار است. درمانهای کنونی شامل داروهای مسکن، فیزیوتراپی و استروئیدها یا تعویض بخش یا کل زانو است. حدود 40 هزار درمان این چنینی در سال در جهان ارائه شده و امید است که با درمان سلولهای بنیادی بتوان آنرا کاهش داد. در حالیکه خود زانو از سلولهای بنیادی برخوردار بوده که قابل تبدیل به سلولهای غضروف هستند، اما تعداد آنها با افزایش سن کمتر شده و کارآیی آنها کاهش مییابد. دانشمندان برای غلبه بر این مشکل، سلولهای بنیادی زانو را استخراج کرده و میزان آنها را در آزمایشگاه پیش از کاشت مجدد آنها در زانو افزایش میدهند. با اینحال این امر نیازمند استخراج و کاشت بوده و به دلیل تعداد محدود سلول بنیادی در دسترس در این اندام، تنها بخشی از آسیب ترمیم میشود.
درمان جدید محققان بر اساس سلولهای بنیادی به دست آمده از خون بند ناف بوده که فعالتر از سلولهای بنیادی بالغ هستند و پژوهشهای حیوانی نشان داده که کارآیی آنها در تولید غضروف بهتر است. خون توسط بانک خون بند ناف جمعآوری میشود. معمولا بندناف پس از وضع حمل دورانداخته میشود اما برخی مادران آنها را برای کمک به پژوهشها اهدا میکنند. سلولهای بنیادی از این اجزا استخراج شده و پس از پرورش در آزمایشگاه به یک ماده ژل مانند تبدیل و سپس توسط جراحان در ناحیه آسیبدیده اعمال میشود. به گفته محققان، این درمان میتواند بخصوص برای افراد سالخورده و بیماران دارای مناطق آسیبدیده بزرگ مورد استفاده قرار گیرد. پس از یک پژوهش کوچک بر روی 10 بیمار در سئول، اکنون دو کارآزمایی قرار است بر روی 50 فرد در دانشگاه راش آمریکا و بیمارستان زنان بریگهام و هفت بیمارستان در کره انجام شود.
..:::: بافت ریه مصنوعی با سلولهای شناور تولید شد ::::..
محققان دانشگاه رایس با استفاده از روش «شناوری مغناطیسی» موفق به کشت سه بعدی سلولها و تولید بافت ریه مصنوعی شدند. بطور سنتی کشت سلولی در پتری دیش انجام می شود، اما سلول های کشت داده شده در این روش مسطح بوده و حالت سه بعدی پیدا نمی کنند. محققان دانشگاه رایس با همکاری مرکز Nano3D Bioscience از فناوری شناوری مغناطیسی (Magnetic Levitation) برای کشت سه بعدی سلولها استفاده کرده و چهار نوع از سلول ها را درون بافت ریه مصنوعی جای دادند.
در این روش، نانو ذرات مغناطیسی بداخل سلولها وارد شده و محققان با کمک یک قلم مغناطیسی موفق به دستکاری سلول ها شدند؛ توانایی دستکاری سلول ها، امکان جدیدی برای کشت های پیچیده فراهم می کند.بافت چهار لایه ریه از سلول های اندوتلیال، سلول های عضله نرم، فیبروبلاست ها و سلول های مخاطی ساخته شد؛ قرار دادن این سلول ها در روشی مشابه بافت طبیعی ریه تاکنون انجام نشده بود و این دقیق ترین و واقعی ترین نمونه بافت مصنوعی برونش محسوب می شود. تولید بافت ریه مصنوعی می تواند به محققان برای شبیه سازی اثر سموم بر روی ریه کمک کرده و به توسعه درمان های جدید و موثر منجر شود.
..:::: درمان سل با درخت مسواک ::::..
نوعی درخت مسواک دارویی در افریقای جنوبی، آنتیبیوتیک جدیدی برای درمان بیماری سل به روشی نوین ارائه میدهد. نوعی ترکیب اشتقاقشده از درخت مسواک در آفریقای جنوبی هدف دارویی مرض سل را به شیوهای ناشناخته غیرفعال میکند. مرض سل بیش از هر بیماری باکتریایی دیگر عامل مرگ در جهان گزارش شده است. بسیاری از داروهای کنونی مقابلهکننده با این مرض حدود 50 سال قدمت دارند و لزوم وجود جایگزینهایی برای آنها احساس میشود.
ترکیب شناسایی شده توسط دانشمندان حاضر در این مطالعه diospyrin نام دارد. این ترکیب به مکان جدیدی بر روی آنزیم مشهور DNA gyrase میچسبد و آن را غیرفعال میکند. آنزیم مزبور برای حیات باکتریها و گیاهان اساسی بوده اما در حیوانات و انسانها وجود ندارد. عنصر DNA gyrase به عنوان یک هدف دارویی موثر و ایمن در مقابل آنتیبیوتیکها عمل میکند. به گفته پروفسور تونی مکسول از مرکز جان اینز و یکی از اعضای تیم تحقیقاتی، شیوه عملکرد diospyrin به توضیح این نکته که چرا این ترکیب در مقابل مواد مقاوم در مقابل داروی سل موثر است، کمک میکند.
در طب سنتی ویژگیهای ضدباکتریایی درخت افریقایی بررسی شده برای سلامتی دهان و درمان برونشیت، ذاتالجنب و بیماریهای مقاربتی به کار میرود؛ همچنین از ترکههای آن به عنوان مسواک استفاده میشود. بسیاری از آنتیبیوتیکها از منابع طبیعی مانند باکتری خاکی Streptomyces گرفته میشوند و آنتیبیوتیکهای استخراج شده از گیاهان کمتر معمول است، با این حال آنها به طور بالقوهای منابع غنی پزشکی نوین هستند.
مطالعه بر روی diospyrin و ترکیبات مرتبط naphthoquinone توسط مکسول و همکارانش به عنوان بخشی از تلاشهای کنسرسیوم محققان اروپایی موسوم به "داروهای بیشتر برای سل" (MM4TB) انجام میشود. این همکاری بین 25 لابراتوار در سراسر اروپا و با هدف توسعه داروهای جدید علیه سل صورت میگیرد. جزئیات این مطالعه علمی در Journal of Biological Chemistry انتشار یافت.
..:::: تولید دارویی برای مقابله با اثرات جانبی درمان سرطان ::::..
دانشمندان دانشگاه لینکوپینگ سوئد موفق به تولید دارویی جدید شدند که بیماران را در مقابل اثرات جانبی درمانهای سرطان مانند شیمی درمانی حفظ کرده و در عین حال نیز اثرات درمانی بر تومورها را افزایش میدهد. به گفته پروفسور "رولف اندرسون"، نویسنده این پژوهش، داروی به دست آمده با نام "calmangafodipir" مبتنی بر مادهای موسوم به "mangafodipir" است که در محیطهای آزمایشی، اثر محافظتی بر سلولهای سالم را در درمانهای سرطان نشان داده است. این ماده میتواند شکل گیری رادیکالهای اکسیژن را که یکی از علتهای بروز اثرات جانبی شیمی درمانی است، تحت تاثیر قرار دهد. برای مثال، این رادیکالها شمار سلولهای سفید خونی را شدیدا کاهش میدهد که در نهایت باعث ابتلای بیمار به عفونتهای گوناگون و حتی مرگ میشود.
طی این پژوهش محققان ابتدا با انجام آزمایش سلولی، گروهی از موشها را به سلولهای سرطانی مبتلا کردند. سپس این موشها را همزمان تحت شیمی درمانی و استفاده از "mangafodipir" قرار دادند. گزارشها نشان میداد که با استفاده از این روش، تشکیل تومورها با حفظ سلولهای سفید خون کاهش یافته بود. تنها مشکل این روش، رها سازی میزان بالایی منگنز از "mangafodipir" بود که اثرات مثبت این روش درمانی را کاهش میداد و علاوه بر این میتوانست به علت ماهیت سمی بودن منگنز، به مغز آسیب برساند.
پژوهشگران برای حل این مشکل، مقدار زیادی از منگنز "mangafodipir" را با کلسیم جایگرین کردند که باعث پایداری بیشتر این ترکیب و افزایش خاصیت محافظتی سلولها و ضد سرطانی آن شد. بر اساس این گزارش، خاصیت اثربخشی "mangafodipir" بر گروه کوچکی از بیماران مبتلا به سرطان روده با موفقیت ثابت شد. این پژوهش در مجله "Translational Oncology" منتشر شده است.
..:::: نخستین کاشت پمپ در بدن برای مبارزه با سرطان ::::..
یک بیمار انگلیسی مبتلا به سرطان به عنوان اولین فرد در جهان در فرآیندی که به باور پزشکان میتواند یک دستاورد بزرگ برای درمان این بیماری باشد، موفق به کاشت یک پمپ در بدن خود شد. به ادعای متخصصان، این تجربه میتواند نقش مهمی را در زندگی هزاران بیمار سرطانی ایفا کند. این پمپ برای خلاصی از مایع خطرناک ساخته شده در بسیاری از سرطانها طراحی شده که میتواند منجر به نیاز به مراجعه کمتر بیمار به بیمارستان شود. در طولانی مدت امید است که این دستگاه بتواند پیگیری شیوههای تغییر سرطان را تسهیل کرده تا پزشکان بتوانند با درمانهای جدید واکنش نشان دهند.
این بیمار انگلیسی یک زن 62 ساله بود که طی یک عمل پیوند یک ساعته در بیمارستان هامراسمیت لندن این پمپ را در زیر پوست خود قرار داد. سرطان تخمدان باعث آزار این بیمار شده بود که مجبور بود هر سه هفته یکبار برای تخلیه چهار تا پنج لیتر از مایع ایجاد شده توسط این بیماری از بدن به بیمارستان مراجعه کند. این مایع بدین معنی است که بیمار قادر به خوردن غذا نبود. حدود یک سوم زنان مبتلا به سرطان تخمدان با مایع آسیت در بدن خود دست و پنجه نرم میکنند که یک تجمع مایع در شکم بوده و بیماران مبتلا به سرطانهای روده، پانکراس، رحم و پستان نیز ممکن است مشکلات مایع را تجربه کنند. در حال حاضر بیماران باید به بیمارستان رفته و در فرآیندی که ممکن است چند روز به طول بینجامد، این مایع را تخلیه کنند. این امر میتواند منجر به مرگ شود.
یک کارآزمایی بالینی کامل قرار است به زودی آغاز شده و این کاشت فعلا بطور دائمی در دسترس نخواهد بود اما در صورت اثبات موفق بودن آن، میتواند درمان بسیاری از سرطانها را با تغییر مواجه کند. دستگاه «alfapump»مایعات را از شکم بیمار به درون مثانه پمپاژ کرده تا از طریق ادرار از بدن خارج شود. پزشکان سپس میتوانند ادرار را برای ارزیابی پیشرفت سرطان و واکنش متعاقب بررسی کنند. این رویکرد بر روی بیماران کبدی آزمایش شده اما این عمل جراحی پیشگامانه نشانگر اولین استفاده از این دستگاه برای درمان سرطان بوده است.
..:::: موفقیت دانشمندان در تعیین میزان پیشرفت سرطان با شیوه پیشگامانه ::::..
محققان دانشگاه کالیفرنیا در ساندیگو توانستند شیوه پیشگامانهای را ابداع کنند که میزان گسترش سرطان در غدد لنفاوی را نشان میدهد. این شیوه که از مولکولهای فلورسنت استفاده میکند، به جراحان اجازه خواهد داد تا غدد لنفاوی سرطانی را شناسایی کرده و بافتهای سالم را نجات دهند. غدد لنفاوی که در سراسر بدن گسترش یافتهاند، نقش مهمی را در کمک به بدن در شناسایی و مبارزه با میکروبها ایفا میکنند. این غدهها به عنوان فیلترهایی عمل میکنند که حاوی سلولهای ایمنی برای مبارزه با عفونت و پاکسازی پوست هستند. هنگامی که سلولهای سرطانی از یک تومور در هر قسمت از بدن جدا میشوند، میتوانند در سیستم لنفاوی حرکت کرده و در این اندام کوچک پنهان شوند. جراحان این غدد را برای اطمینان از امکان گسترش سرطان و میزان آن برمیدارند.
با این حال در زمان جراحی شناسایی غدد انسان با اندازه کمتر از نیم سانتیمتر در میان بافت اطراف آن مشکل است. حتی اگر جراحان بتوانند موقعیت غده را مشخص کنند، هیچ شیوهای برای نمایش امکان سرطانی بودن یا نبودن آنها وجود نداشته و نیازمند حذف تعداد غدد لنفاوی بیشتر از حد ضروری است. اما این شیوه جدید بسیار حساس بوده و میتواند محل سلولهای سرطانی با اندازه چند میلیمتری را نیز شناسایی کند.
به گفته محققان، این ابزار باعث ارتقای میدان دید جراح تا حدی میشود که هیچ توموری ندیده باقی نمیماند. مولکولهای با برچسب فلورسنت موسوم به RACPP قابل تزریق هستند. جراحان با استفاده از این مولکولها در مدلهای موش توانستند محل گسترش سرطان را مشاهده کرده و مناطق میلیمتری را حتی با حساسیت بیشتر ببینند. در حال حاضر پزشکان تنها میتواند محل غدد لنفاوی را بدون توانایی تشخیص سرطانی بودن یا نبودن آنها شناسایی کنند. شیوههای کنونی برای کنترل سرطان پروستات شامل برداشتن تمام غدد لنفاوی مشکوک پیش از شناسایی میزان پیشرفت سرطان است. نتایج این پژوهش در مجله Cancer Research منتشر شده است.
..:::: ساخت دوربین بلعیدنی برای شناسایی مراحل ابتدایی سرطان مری ::::..
محققان بیمارستان عمومی ماساچوست، نوعی دوربین قرصی بلعیدنی را ساختهاند که میتواند به پزشکان در تشخیص نشانههای اولیه سرطان مری کمک کند. این دستگاه شفاف فناوری پیشرفته، به اندازه یک قرص مولتی ویتامین بزرگ بوده و حاوی لیزری با سرعت چرخش بالاست که یک پرتو نور نزدیک مادون قرمز را به دیواره مری میتاباند. سپس حسگرها بازتاب نور را ثبت کرده و تصاویر دقیق میکروسکوپی را تولید میکنند که میتواند تغییرات سلولی مرتبط با سندروم «بارت» را که شرایط پیش سرطانی مرتبط با سوزش سردل و رفلکس اسید است، آشکار سازد.
یک نوار نخ مانند به دستگاه اجازه میدهد تا به عقب کشیده شده و تصاویر را به یک مانیتور منتقل کند. این دستگاه بر روی 13 داوطلب بدون بیهوشی آزمایش شد که شش مورد از آنها به سندروم بارت مبتلا بودند. این کپسول توانست کل مری را در کمتر از یک دقیقه تصویربرداری کند. یک فرآیند کامل که شامل چهار مسیر بالا و پائین مری بوده، تنها شش دقیقه طول کشید. ارزیابیهای کنونی برای این بیماری بیش از یک ساعت به طول انجامیده و شامل استفاده از آندوسکوپی در گلوی بیمار است. این دستگاه جدید به نمایش ساختارهای زیرسطحی غیرقابل مشاهده با آندوسکوپی پرداخته و بطور واضح میتواند نشانههای سندروم بارت را شناسایی کند.
اگرچه در ابتدا نگرانیهایی در مورد امکان مفقود شدن اطلاعات به دلیل کوچک بودن مقیاس دستگاه وجود داشت، اما آزمایشات نشان داده که این نگرانیها بیمورد است. با بلع این قرص، مری آنرا به شکل محکم گرفته و تصویربرداری کامل از دیواره این اندام را ممکن میسازد. سندروم بارت در اثر مواجهه مزمن مری با اسید بالا آمده از معده ایجاد شده که منجر به تحریک و سوزش سر دل میشود. یکی از هر 10 بیمار دچار رفلکس اسید معده به این سندروم دچار خواهند شد که سهم مردان در این میان بیشتر است. این پژوهش در مجله Nature Medicine منتشر شده است.
..:::: مصرف مکمل های روغن ماهی اثرات آلودگی هوا را کاهش می دهد ::::..
آلودگی هوا ترکیبی از گازها و ذرات کوچکی از مواد جامد و مایع است. میلیاردها نفر در سراسر جهان در مناطقی زندگی می کنند که در آنجا هوا به شدت آلوده است. مطالعه مردمی که در معرض آلودگی هوا قرار دارند نشان می دهد که ذرات ریز آلاینده موجود در هوا به بروز مشکلات سلامتی مختلفی از قبیل آسم، سکته مغزی، آریتمی و نارسایی قلبی منجر می شود. تصور می شود که ذرات ریز آلاینده موجود در هوا موجب تغییر سطح لیپید در خون می شود. همچنین شواهد متقنی وجود دارد که این ذرات ریز باعث افزایش بیماری های قلبی عروقی و مرگ و میرهای ناشی از آن می شود.
این اولین مطالعه ای است که ارتباط میان مصرف مکمل های روغن ماهی و کاهش اثرات آلودگی هوا بر قلب را بررسی می کند و نشان می دهد که ایجاد اندک تغییراتی در رژیم روزانه غذایی می تواند برخی اثرات آلودگی هوا بر سلامت را خنثی کند. یافته های این مطالعه برای افرادی که در مناطقی از جهان زندگی می کنند که آلودگی هوا در آنجا شدید است مهم است. این مطالعه نشان داد که ضربان قلب و سطح لیپید افرادی که مدت یک ماه مکمل های روغن ماهی مصرف کرده بودند و در معرض هوای آلوده زندگی می کردند تغییرات اندکی پیدا کرده بود. ضربان قلب و سطح لیپید دو مقایس اندازه گیری سلامت قلب هستند.
محققان در این مطالعه 29 فرد 50 تا 72 ساله را به دو دسته تقسیم کردند و برای مدت یک ماه به یک گروه مکمل روغن زیتون و به گروه دیگر مکمل روغن ماهی دادند. این افراد در محیطی مورد مطالعه قرار گرفتند که هوا به شدت آلوده بود. این افراد سالم بودند و سابقه دیابت، بیماری قلبی عروقی و یا ریوی نداشتند. همچنین این افراد دست کم یک سال سیگار نکشیده بودند. این مطالعه نشان می دهد، پس از قرار گرفتن در معرض سطوح شدید هوای آلوده ضربان قلب افرادی که مکمل های روغن زیتون مصرف کرده بودند به اندازه قابل توجهی کاهش یافت. در عوض افرادی که مکمل های روغن ماهی مصرف کرده بودند تغییرات کمی در ضربان قلب آنها مشاهده شد. محققان همچنین متوجه شدند گروهی که روغن زیتون مصرف کرده بودند پس از قرار گرفتن در معرض هوای آلوده سطح دو نوع لیپید در خون آنها افزایش یافت، در حالی که این افزایش در گروهی که مکمل روغن ماهی مصرف کرده بودند محسوس نبود.
این اولین مطالعه ای است که نشان می دهد مصرف روغن ماهی می تواند علائم قلبی عروقی ناشی از قرار گرفتن در معرض هوای آلوده را کاهش دهد. نتایج این مطالعه مدرک محکم تری نسبت به مطالعاتی که تا کنون انجام شده است در زمینه نقش روغن ماهی در کاهش اثرات قلبی عروقی ناشی از آلودگی هوا ارائه می دهد. این یافته برای افرادی که در شهرها و مناطقی زندگی می کنند که کیفیت هوای خوبی ندارند حائز اهمیت است. روغن ماهی مملو از اسیدهای چرب غیر اشباع امگا 3 است که گفته می شود از کاهش ضربان قلب ناشی از قرار گرفتن در معرض هوای آلوده پیشگیری می کند. کاهش ضربان قلب با مرگ و ابتلا به آریتمی ارتباط دارد. نتایج این مطالعه نشان می دهد که اقدام شخصی مصرف روزانه کپسول روغن ماهی می تواند یک استراتژی مقرون به صرفه برای محافظت از سلامتی باشد.
..:::: درمان آسم با چسب کنه! ::::..
محققان فرانسوی چسب حاوی پروتئین کنه تولید کردهاند که میتواند به درمان بیماری آسم کمک کند. کنه گرد و غبار خانگی (house dust mite) یک حشره نیم میلی متری است که در بالش، تشک، ملحفه ها، لباس یا فرش تجمع می کند. هنوز ارتباط مستقیم آسم با کنه گرد و غبار خانگی مشخص نشده است، اما به نظر می رسد که پروتئین موجود در مدفوع این موجود باعث بروز حملات آسم می شود؛ این پروتئین موجب تحریک سیستم ایمنی برای تولید آنتی بادی هایی می شود که مقادیر زیادی هیستامین در بدن ترشح می کنند. ترشح بیش از حد هیستامین باعث تورم و سوزش راه های هوایی، مشکلات تنفسی و حملات آسم می شود.
محققان شرکت DBV Technologies چسبی حاوی نمونه تولید شده پروتئین مدفوع کنه را توسعه داده اند که می تواند بعنوان یک روش موثر برای درمان آسم مورد استفاده قرار بگیرد. در شیوه درمانی ایمونوتراپی یا حساسیت زدایی، سیستم ایمنی بصورت تدریجی در معرض مقادیر کمی از پروتئین عامل بروز حساسیت قرار گرفته و مجددا تنظیم می شود که در این حالت دیگر پروتئین را بعنوان یک عامل تهدید کننده نمی شناسد. فرآیند آموزش سیستم دفاعی بدن برای عدم واکنش به مدفوع کنه، چندین ماه بطول می انجامد و پس از این مدت دیگر نیازی به استفاده از چسب بر روی پوست نیست.
کپسول های ریز درون چسب ViaSkin حاوی نمونه پروتئین مدفوع کنه، روی دست یا شکم قرار گرفته و بتدریج مقادیر محدودی از پروتئین را در روی پوست منتشر می کند که باعث تنظیم مجدد سیستم ایمنی بدن می شود. پس از طی کردن دوره درمان، زمانیکه فرد در معرض مدفوع کنه (بعنوان آغاز کننده حملات آسم) قرار بگیرد، واکنش حساسیت زایی در بدن ایجاد نمی شود. این چسب علاوه بر درمان مبتلایان به آسم حاد می تواند برای پیشگیری از توسعه مراحل اولیه بیماری در کودکان نیز مورد استفاده قرار بگیرد. نخستین آزمایش بالینی چسب ViaSkin بر روی انسان اوایل سال آینده میلادی آغاز می شود؛ محققان این شرکت در حال حاضر از همین فناوری برای تولید چسب ضد حساسیت شیر و بادام زمینی استفاده می کنند.
..:::: اختراع دستگاهی برای پمپاژ معده در چاقی مرضی ::::..
یک شرکت آمریکایی به معرفی اختراعی پرداخته که میتواند برای درمان چاقی مرضی، بدون نیاز به جراحی تهاجمی و معایب بایپس معده، امیدبخش باشد. سیستم جدید شرکت Aspire Bariatrics به بیماران اجازه میدهد تا هر چقدر میل دارند غذا بخورند، سپس شکم آنها را حدود 20 دقیقه پس از صرف غذا با اتصال یک پمپ به سوپاپی که طی یک عمل جراحی در دیواره شکم آنها نصب شده، زهکشی میکند. اگرچه این سیستم هنوز توسط سازمان غذا و داروی آمریکا تائید نشده، اما در کارآزماییهای بالینی اولیه آن، برخی بیماران از کاهش وزن تا 20 کیلوگرم در یک سال و برخی دیگر حتی به میزان دو برابر گزارش کردهاند. بخشی از این اختراع ، محصول ایده «دین کامن» است که در حوزه ساخت دستگاههای پزشکی فعال است.
این شیوه از بسیاری از جراحیهای مختلف بای پس معده کمتر تهاجمی بوده و میتواند به بیماران در جلوگیری از برخی از تاثیرات عجیب هورمونی و روانی که برخی از بیماران پس از عمل جراحی تجربه میکنند، کمک کند. البته این دستگاه نیاز به تغییرات بیشتر برای کاربردیتر شدن دارد. برای مثال از جمله اشکالات این دستگاه این است که بیمار باید لوله پمپ را برای افزایش نیروی محرکه و تجزیه غذاهای بزرگتر فشار دهد. همچنین رژیم غذایی فرد نیز باید کنترل شده باشد.
..:::: ساخت روباتی که استفراغ میکند! ::::..
دانشمندان انگلیسی یک روبات استفراغ کننده پرتابهای را طراحی کردهاند که به آنها در بررسی چگونگی انتقال بیماری نورو ویروس که این کشور را فرا گرفته، کمک خواهد کرد. سیستم روبات انساننمای «لری» برای هفتههای متمادی در آزمایشگاه امنیت و سلامت دربیشایر در حال استفراغ بوده تا دانشمندان بتوانند میزان پرتاب ترشحات بیماری آن را بررسی کنند. پرتابههای این روبات که توسط «کاترین مکیسون» ساخته شده، به راحتی قابل شناسایی است؛ چرا از یک جایگزین ماده قیشده فلورسنت برای تشخیص حتی کوچکترین ترشحات تشکیل شدهاند. اما در جهان واقعی، پیگیری میزان عفونت در این بیماری مسری که در حال انتشار بوده، بسیار سخت است.
به گفته دانشمندان، نورو ویروس یکی از مسریترین ویروسهای شناخته شده برای انسان است. کمتر از 20 ذره ویروس برای آلوده کردن فرد کافی است؛ از این رو هر قطره از استفراغ یا میزان کم مدفوع فرد بیمار میتواند از ویروس کافی برای ابتلای بیش از 100 هزار فرد سالم برخوردار باشد. این ویروس امسال با قدرت بیشتری وارد شده و تنها در انگلیس بیش از یک میلیون فرد به اسهال و استفراغ شدید مبتلا شدهاند.
نورو ویروس که بیش از 40 سال پیش شناسایی شده، نام خود را از شهر نورواک آمریکا گرفته که در سال 1968 بیماری اسهال حاد در میان کودکان مدرسه آن شایع شده بود. نشانههای این بیماری شامل استفراغ ناگهانی به شکل پرتابی و اسهال به شکل شدید و آبکی است. برخی از مبتلایان همچنین به تب، سردرد و گرفتگی عضلات معده دچار میشوند. آنچه این ویروس را به یک دشمن نیرومند تبدیل کرده، قابلیت آن برای مقاومت در برابر پاکسازی و تحمل دورههای طولانی در خارج از بدن میزبان انسانی است. دانشمندان دریافتهاند که این ویروس میتواند برای 12 ساعت در سطح سخت و 12 روز در پارچه آلوده مانند فرش و اثاث درون منزل زنده بماند. از دیگر قابلیتهای این ویروس میتوان به این امر اشاره کرد که میتواند در آب ساکن برای چندین ماه و حتی چند سال زنده بماند. نورو ویروس همچنین در برابر مواد ضدعفونی کننده خانگی و حتی الکل و ژل مقاوم است. از آنجایی که هنوز واکسن و درمان خاص برای پیشگیری از این بیماری وجود ندارد، محققان توصیه کردهاند که از افراد مبتلا به این ویروس دوری کرده و بطور منظم از آب و صابون استفاده کنند.
..:::: تولید سلولهای قاتل سرطان ::::..
محققان ژاپنی برای نخستین بار موفق به تولید سلولهای قاتلی شدهاند که با تزریق به بدن بیمار میتوانند سلول های سرطانی خاص را نابود کنند. بدن انسان حاوی سلول های ایمنی برنامه ریزی شده برای مقابله با سرطان و عفونت های ویروسی است، اما تعداد کم و عمر کوتاه این سلول ها باعث ناکامی در مقابله با بیماری های تهاجمی مانند سرطان و ایدز می شود. محققان مرکز تحقیقات آلرژی و ایمونولوژی RIKEN ژاپن به سرپرستی پروفسور «هیروشی کاواموتو» برای نخستین بار با استفاده از فناوری سلول های بنیادی، موفق به بازسازی سلول های ایمنی بدن و تولید تعداد فراوانی سلول قاتل شدند. این سلول های سیستم ایمنی، لنفوسیت های تی قاتل (T lymphocytes) نامیده می شوند.
مطالعه قبلی نشان می دهد، لنفوسیت های تی تولید شده در آزمایشگاه با استفاده از شیوه های متداول، بدلیل عمر کوتاه نمی توانند برای از بین بردن سلول های سرطانی مورد استفاده قرار بگیرند. محققان برای غلبه بر این مشکل و تولید لنفوسیت های تی موثر، نخست آنها را به نوع دیگری از سلول موسوم به سلول بنیادی قلب و نخاع القا شده (iPS) تبدیل کردند. لنفوسیت تی بازسازی شده از سلول های iPS از عمر طولانی برخوردار بوده و می توانند سلول های سرطانی خاص را در بدن بیمار شناسایی کرده و از بین ببرند. محققان امیدوارند با تزریق شمار زیادی از سلول های لنفوسیت های تی قاتل به بدن بیماران، سیستم ایمنی را برای مقابله با سلول های سرطانی تقویت کنند؛ این شیوه می تواند در آینده برای درمان های جدید انواع سرطان و ایدز مورد استفاده قرار بگیرد. نتایج این مطالعه در مجله Stem Cell منتشر شده است.
..:::: کشف علت دردهای عضلانی استاتین درمانی ::::..
دانشمندان دریافتند که مکانیزم پنهانی در پس اثرات جانبی استاتین درمانی وجود دارد که موجب دردهای عضلانی میشود. در حال حاضر استاتینها پرمصرف ترین داروهای کاهش کلسترول (LDL) هستند که با مهار توانایی کبد، از تولید کلسترول جلوگیری میکنند. از اثرات جانبی استاتین درمانی، درد عضلانی است که 75 درصد مصرف کنندگان نیز آن را تجربه میکنند. این درد ممکن است مردم را از ادامه استاتین درمانی یا ورزش کردن دور کند که هر دوی این پیشامدها، برای این دسته از بیماران مضر است. پرفسور "فلمینگ دلا"، محقق دانشگاه کوپنهاگ دانمارک با اشاره به نتایج تحقیق انجام شده در این رابطه میگوید: اکنون محققان این پژوهش نشان دادهاند که استاتین درمانی، تولید انرژی در عضله را تحت تاثیر قرار میدهد و گمان دانشمندان نیز بر این است که این مکانیزم باعث ضعیف شدن ماهیچه و در نتیجه احساس درد میشود. علاوه بر این پژوهشگران دریافتند در بدن بیمارانی که تحت استاتین درمانی قرار میگیرند، میزان پایینی از پروتئین "Q10,Q10" وجود دارد که موجب کاهش انرژی تولیدی در عضله شده و میتواند به عنوان علت بیولوژیک درد این بیماران در نظر گرفته شود. این پژوهش در مجله "American College of Cardiology" منتشر شده است.
..:::: تراشه جیبی برای انجام 50 آزمایش خون ::::..
با استفاده از تراشه سبک و قابل حمل V-Chip امکان انجام طیف وسیعی از آزمایشهای خون در کمتر از یک دقیقه و در هر مکانی فراهم میشود. انجام آزمایش خون در آزمایشگاه، روشی هزینه بر محسوب میشود، اما تراشه نوار نمودار حجمی (V-Chip) تنها با استفاده از یک قطره خون، انجام 50 آزمایش مختلف را امکان پذیر میکند. یک قطره خون بر روی کانال زیگ زاگی بین دو صفحه شیشهای کوچک ریخته میشود؛ در بالای کانال 50 حفره قرار دارد که هرکدام حاوی پراکسید هیدروژن، رنگ، آنزیم و انواع مختلف آنتی بادی، پروتئین،DNA یا RNA موردنظر است. بطور مثال برای تبدیل یکی از حفرهها بعنوان آشکارساز انسولین، این حفره با آنتی بادی انسولین پیش بارگذاری می شود.
زمانیکه یک نمونه حاوی انسولین بر روی تراشه قرار می گیرد، این آنتی بادیها باعث فعال شدن آنزیمی می شوند که اکسیژن را از پر اکسید هیدروژن جدا می کند و اکسیژن با تغییر سطح رنگ، سطح انسولین در نمونه را مشخص می کند. کاربر می تواند نتیجه آزمایش را مانند یک نمودار میله ای با استفاده از یک مقیاس دستی در کنار تراشه مشاهده کند. اگرچه این روش از لحاظ سطح صحت و حساسیت مانند تست های آزمایشگاهی نیست، اما می توان در شرایط اضطراری مانند مسمومیت با مواد مخدر (اوردوز) از این تراشه استفاده کرد. این تراشه سبک و با کاربری ساده با قیمت 10 دلار به بازار عرضه شده است.
..:::: کشف دو ژن که خطر ابتلا به سرطان روده را افزایش میدهند ::::..
محققان انگلیسی به تازگی موفق به کشف دو ژن شدهاند که از والد به فرزند منتقل میشود و به طور قابل توجهی خطر تشکیل تومور سرطان روده را افزایش میدهد. دانشمندان دانشگاه آکسفورد و مؤسسه تحقیقات سرطان در لندن مدعیاند با این کشف خواهند توانست دلیل آسیبپذیری خانوادهها در مقابل این نوع سرطان را توضیح دهند. آنها در مطالعاتشان دی ان ای 20 بیمار مبتلا به سرطان روده و دارای سابقه خانوادگی ابتلا به آن را مورد بررسی قرار دادند. این متخصصان با مطالعه کد ژنتیکی نمونه موردیهای مزبور به خطاهایی در دو ژن پی بردند که شانس ابتلا به این بیماری مهلک را افزایش میدهد. به گفته آنها، در این مطالعه افراد دارای نسخه اشتباه POLE یا POLD1 به سرطان روده مبتلا بودند یا یک رشد پیشسرطانی را در رودههایشان داشتند. دانشمندان سپس چهار هزار بیمار مبتلا به سرطان مزبور و شش هزار و 700 فرد سالم را بررسی کردند و دریافتند که این جهشها در هیچ یک از افراد سالم حاضر در نمونه موردی مشاهده نشدند. به گفته «ایان توملینسون» رهبر ارشد تیم تحقیقاتی، این جهشها نادرند اما وجود یکی از آنها برای ابتلا به سرطان روده کافی است. جزئیات این مطالعه در Nature Genetics انتشار یافت.
تاییدیه149- سيگنيفور
سازمان غذا و داروي آمريکا (FDA) اخيرا پازيرئوتايد دياسپارتات(pasireotide diaspartate) با نام تجاري سيگنيفور (Signifor) را براي درمان کوشينگ در بيماراني که جراحي به آنها کمکي نخواهد کرد، مورد تاييد قرار داده است. بيماري کوشينگ به دنبال توليد بيش از حد کورتيزول از غدد آدرنال ايجاد ميشود. وجود تومور در غده هيپوفيز باعث تحريک بيشتر غده آدرنال و در نتيجه توليد بيش از حد کورتيزول ميشود. کورتيزول فعاليتهاي مهمي را در بدن تنظيم ميکند. (از جمله پاسخدهي به استرس و صدمه). مبتلايان به کوشينگ در معرض خطر اضافه وزن، ديابت يا عدم تحمل گلوکز، فشارخون بالا و عفونت هستند. ايمني و اثربخشي سيگنيفور در يک مطالعه باليني با شرکت 162 بيمار مبتلا به کوشينگ مورد بررسي قرار گرفت. شرکتکنندگان در اين مطالعه بهطور تصادفي يکي از دو دوز سيگنيفور را طي 6 ماه درمان دريافت کردند. به برخي از بيماران با پاسخدهي درماني مطلوب اجازه ادامه درمان داده شد. سيگنيفور باعث کاهش سطح کورتيزول در ادرار 24 ساعته ميشود. اين کاهش در يک ماه پس از شروع درمان ديده شد. ميزان کورتيزول ادرار در حدود 20درصد از بيماران تحت مطالعه به سطح طبيعي رسيد. سيگنيفور باعث افزايش سطح قند خون ميشود بنابراين ادامه درمان با اين دارو ممکن است باعث وخيمتر شدن ديابت در برخي از بيماران شود. به همين دليل FDA انجام مطالعات پس از ورود به بازار مصرف را براي اين دارو درخواست کرده است. سيگنيفور 2 بار در روز زير پوست تزريق ميشود.
..:::: کاهش گسترش سلولهای سرطانی با هدف قرار دادن پروتئینی خاص ::::..
محققان دانشگاه ایالتی پنسیلوانیا طی پژوهشی دریافتند که میتوان گسترش سلولهای سرطانی را با هدف قرار دادن پروتئینی محرک موسوم به "km23-1" که در حرکت و جابهجایی سلولی نیز دخیل است، کاهش داد. حرکت سلولی جنبه مهمی در فرآیند گسترش یک تومور است. تغییرات به وجود آمده طی این فرآیند میتواند سلول تومور را از سلولهای محلی، غیرتهاجمی و محدود به سوی سلولهای سرطانی متاستاتیک (جا به جا شونده) انتقال دهد. سلولها با استفاده از پروتئین اکتین که چارچوب ساختاری سلول را میسازد، در بدن حرکت میکند. اکتین با ایجاد رشتههایی از فیبرهای ریسمانی شکل بر لبه سلول، برآمدگی را در غشای سلول به وجود میآورد که باعث به جلو راندن سلول میشود. چندین پروتئین شناخته شده، سازماندهی مجدد چارچوب سلول را تنظیم میکنند که نشان داده شده است این پروتئینها در بعضی سرطانها نیز فعالتر هستند.
براساس این پژوهش، بیان بیش از حد "km23-1" تشکیل فیبر اکتین را افزایش میدهد. زمانی که "km23-1" کاهش یابد، فعالیت "RhoA" تقلیل پیدا میکند. "RhoA" سوییچ مهمی است که فعالیتهای دخیل در جا به جایی سلول را فعال میکند. به گفته "مولدر" با مشاهده این فرآیندها میتوان چنین گفت که "km23-1" برای تنظیم این سوییچها لازم بوده و در جابهجایی سلولی نیز نقش دارد و با مهار این پروتئین، رویدادهای سهیم در گسترش سلولی به سایر نقاط بدن نیز مسدود میشود. وی در ادامه میگوید: زمانی که در نمونه سلولهای سرطانی روده "km23-1" کاهش یافت، مهاجرت سلولهای سرطانی نیز کاهش یافت. بنابر این گزارش، تحقیقات زیادی برای درک این فرآیندها لازم است اما "km23-1" میتواند هدفی امیدبخش برای تولید داروهای ضد متاستاتیک و درمانهای سرطانی باشد. این پژوهش در مجله "Biochemical and Biophysical Research Communications" منتشر شده است.
..:::: سیگاریها حداقل 10 سال کمتر عمر میکنند ::::..
تحقیقات حاکیست که عدم استعمال دخانیات به ویژه در زنان باعث افزایش طول عمر میشود. نتایج یک مطالعه طی 23 سال روی 70 هزار شهروند هیروشیما و ناکازاکی نشان داده است که استفاده نکردن از سیگار و سایر دخانیات در حدود 10 سال به عمر افراد میافزاید. 72 درصد از مردان سیگاری موجود در این مطالعه که از 20 سالگی اقدام به کشیدن سیگار کرده بودند تا 70 سالگی عمر کردند که در این میان مردانی که هیچگاه سیگار، مصرف نکردند تا 8 سال بیشتر زندگی کردند. نتایج حاصل از این تحقیق با بررسی زنان موجود در این مطالعه افزود 79 درصد از زنانی که از 20 سالگی سیگار کشیدن را آغاز کرده بودند تا 70 سالگی عمر کردند که در بین زنان مورد مطالعه افرادی که هیچگاه به سیگار کشیدن روی نیاوردند تا 80 سالگی عمر کردند. یافتههای دیگر این مطالعه با مشاهدات بیشتر همچنین افزود: در مقایسه با افراد سیگاری دیگر افرادی که قبل از 35 سالگی مصرف سیگار را قطع کرده بودند، توانستند بسیاری از مضرات و عوارض حاصل از استعمال دخانیات را در خود کاهش دهند و نیز باعث افزایش میزان عمر خود شوند. یافتههای این تحقیق در نشریه BMJ منتشر شده است.
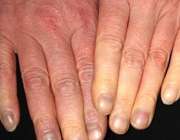
 گرفتگی غیرعادی رگ های خونی باعث کاهش جریان خون به بافت های موضعی می شود و در نتیجه رنگ پوست تغییر می کند.
گرفتگی غیرعادی رگ های خونی باعث کاهش جریان خون به بافت های موضعی می شود و در نتیجه رنگ پوست تغییر می کند.